Il solfato di calcio è un composto inorganico con formula chimica CaSO4 e relativi idrati. La sua caratteristica principale è la capacità di formare idrati, ovvero di assorbire molecole d'acqua. Tutte le sue forme sono solidi bianchi scarsamente solubili in acqua.
Il solfato di calcio provoca una durezza permanente nell'acqua. La sua formula chimica base è CaSO4, ed è il sale di calcio dell'acido solforico.
Forme e Proprietà
Il solfato di calcio si presenta in diverse forme:
- Anidrite (forma anidra): Viene usata come essiccante. Con il riscaldamento a 180 °C, viene prodotta la forma quasi priva di acqua, chiamata anidrite (CaSO4 · 0H2O, dove la quantità di acqua può variare leggermente). L'anidrite reagisce lentamente con l'acqua per tornare allo stato diidrato, una proprietà sfruttata in alcuni disseccanti commerciali. Per riscaldamento sopra i 250 °C si forma la forma completamente anidra chiamata anidrite o anidrite "naturale".
- Gesso di Parigi (emiclase): Un particolare idrato, meglio conosciuto come gesso di Parigi, si ottiene con un attento riscaldamento del gesso, convertendolo nel minerale parzialmente disidratato chiamato bassanite o gesso di Parigi. Questo materiale ha la formula CaSO4 · ½H2O. Temperature comprese tra 100 e 150 °C sono necessarie per allontanare l'acqua all'interno della sua struttura. I valori esatti della temperatura e del tempo dipendono dall'umidità ambientale.
- Gesso minerale (diidrato): Un altro idrato si trova naturalmente come gesso minerale, con formula CaSO4 · 2H2O.
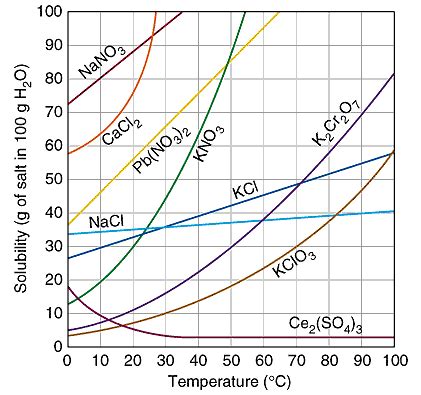
La dissoluzione delle diverse fasi cristalline del solfato di calcio in acqua è esotermica e rilascia calore (diminuzione dell'entalpia: ΔH < 0). Questo comportamento di solubilità controintuitivo, in cui la solubilità diminuisce all'aumentare della temperatura (solubilità retrograda), è dovuto al fatto che la reazione di dissoluzione cede calore. Come immediata conseguenza, per procedere, la reazione di dissoluzione ha bisogno di dissipare questo calore che può essere considerato come un prodotto della reazione. Se il sistema è raffreddato, l'equilibrio di dissoluzione evolverà verso destra secondo il principio di Le Chatelier e il solfato di calcio si dissolverà più facilmente. Se la temperatura del sistema aumenta, il calore di reazione non può dissiparsi e l'equilibrio regredisce verso sinistra secondo il principio di Le Chatelier; la solubilità del solfato di calcio diminuisce all'aumentare della temperatura.
Applicazioni Industriali
Il solfato di calcio ha numerose applicazioni in svariati settori industriali:
Edilizia
Una delle principali applicazioni industriali del solfato di calcio è il suo ruolo nell’edilizia nella realizzazione dello stucco, dove viene impiegato per la decorazione e il rivestimento di muri e soffitti; il solfato di calcio polverizzato e calcinato forma infatti una pasta modellabile quando idratato, indurendosi poi in tempi brevi. Analogamente, viene impiegato per risolvere i problemi relativi all’idratazione del calcestruzzo, divenendo così fondamentale per l’edilizia civile e industriale e delle infrastrutture.
Nell'industria edile, il solfato di calcio viene utilizzato in diverse formulazioni di malta, dove conferisce un effetto di colore bianco, scorrevolezza e una presa/essiccazione più rapida. Il gesso conferisce un certo grado di resistenza al fuoco ai prodotti in cartongesso e le fibre di vetro vengono aggiunte per migliorare questo effetto. Il gesso ha una bassa conducibilità termica, che conferisce all'intonaco alcune proprietà isolanti. Nell'edilizia, i blocchi di gesso sono utilizzati come i blocchi di cemento. La malta di gesso è un'antica malta utilizzata nella costruzione di edifici. È un componente del cemento Portland utilizzato per evitare che il calcestruzzo indurisca (si solidifichi troppo rapidamente).
La proprietà endotermica della reazione di idratazione del gesso è rilevante per le prestazioni del cartongesso, conferendo resistenza al fuoco a strutture residenziali e di altro tipo. In caso di incendio, la struttura dietro un foglio di cartongesso rimarrà relativamente fresca poiché l'acqua viene persa dal gesso, prevenendo così (o sostanzialmente ritardando) danni all'intelaiatura (attraverso la combustione di elementi in legno o la perdita di resistenza dell'acciaio alle alte temperature) e conseguente crollo strutturale.
Agricoltura
In agricoltura, il solfato di calcio ha impiego come fertilizzante, dove contribuisce all’approvvigionamento di calcio per le radici delle piante; e la sua applicazione contrasta anche fenomeni quali la putrefazione delle radici dell’arachide, o il marciume apicale di prodotti quali il pomodoro.
Il gesso fornisce i due macroelementi secondari della pianta, il calcio e lo zolfo. A differenza del calcare, in genere non influisce sul pH del terreno e può quindi essere utilizzato per tutti i tipi di piante. Per migliorare i terreni salini, indipendentemente dal pH, si aggiunge solfato di calcio ai terreni sodici (salini) e acidi, convertendo la forma altamente solubile del boro (metaborato di sodio) nel meno solubile metaborato di calcio. Il gesso riduce la tossicità dell'alluminio e del boro nei terreni acidi. Inoltre, migliora la struttura del suolo, l’assorbimento dell’acqua e l’aerazione.
Medicina e Odontoiatria
In medicina, il solfato di calcio viene utilizzato come eccipiente nella produzione di compresse, ma soprattutto per immobilizzare le articolazioni a seguito di una frattura ossea o una lussazione; mentre in odontoiatria funge da base per la realizzazioni di impronte dentali, protesi e restauri.
Il solfato di calcio ha una lunga storia di utilizzo in odontoiatria. È stato utilizzato nella rigenerazione ossea come materiale da innesto e legante/estensore per innesto e come barriera nella rigenerazione guidata dei tessuti. È un materiale insolitamente biocompatibile e viene completamente riassorbito dopo l'impianto.
La reazione esotermica dell'idratazione del solfato di calcio è responsabile della facilità con cui il gesso può essere colato in varie forme tra cui fogli (per cartongesso), bastoncini (per gesso da lavagna) e stampi (per immobilizzare ossa rotte o per colate di metallo). Mescolato con polimeri, è stato utilizzato come cemento per la riparazione ossea.
Ceramica
In ceramica, il solfato di calcio viene utilizzato come gesso per la costruzione di stampi e la modellazione, nella costruzione di stampi (per ceramica e altri prodotti), come base per il gesso secco e per speciali miscele di aggregati a base di gesso.
Come materiale per la scultura, l'alabastro (una forma di solfato di calcio) è stato particolarmente utilizzato nel mondo antico fino allo sviluppo dell'acciaio, quando la sua relativa morbidezza lo rendeva molto più facile da scolpire. Nel Medioevo era utilizzato da scribi e miniatori come ingrediente del gesso, usato per le lettere miniate e per la doratura dei manoscritti miniati.
Il gesso si ottiene da solfato di calcio sintetico di alta qualità e di colore chiaro e presenta un'elevata stabilità finale rispetto ai tipici emiidrati. Può essere utilizzato come base per lo stucco di gesso. Le proprietà più importanti del gesso sono: molto leggero, contenuto molto basso di additivi non solfati, macinazione di alta qualità (soprattutto fine), alta reattività, assenza di additivi, alta stabilità finale.
Industria Alimentare
Nell'industria alimentare, il solfato di calcio è presente come coagulante nel Tofu (cagliata di soia). Nella produzione di birra, viene utilizzato come regolatore della durezza dell'acqua e come fonte di calcio per le colture di lievito. Nell'industria pasticcera, il solfato di calcio viene utilizzato nei prodotti da forno come condizionatore dell’impasto, per ridurre l’appiccicosità e come fonte di calcio dietetico per i prodotti da forno. Viene utilizzato nella coltivazione dei funghi come fonte di minerali. In alcuni casi viene utilizzato nella produzione di cereali in condizioni di umidità per evitare che i chicchi si agglomerino. Riduce il pH del menthal e aumenta la durezza fissa dell'acqua (ioni calcio). 1 g/10 l aumenta il livello di sale di 23 ppm di calcio e 56 ppm di solfato e aumenta la durezza fissa dell'acqua di 58 ppm.
Trattamento delle Acque
Nel trattamento delle acque, il solfato di calcio viene utilizzato come legante per gli elementi pesanti (piombo, arsenico, ecc.) nel trattamento delle acque e delle acque reflue. Forma composti complessi insolubili, facendo precipitare gli elementi pesanti insieme ai sedimenti e rendendoli inattivi. Questo metodo è utilizzato per il basso costo e la bassa tossicità del solfato di calcio.
Altre Applicazioni
Piccole quantità di gesso calcinato vengono aggiunte alla terra per creare strutture resistenti direttamente dalla terra colata, un'alternativa all'adobe (che perde la sua forza quando è bagnato).
Nell'alluminotermia, a temperature più elevate il solfato di calcio rilascia ossigeno e agisce come agente ossidante.
I risultati del 2011 del rover Opportunity sul pianeta Marte mostrano una forma di solfato di calcio in una vena sulla superficie.
Solfato ammonico top o flop? La risposta scientifica
Fonti e Produzione
Le principali fonti di solfato di calcio sono il gesso e l'anidrite presenti in natura, che si trovano in molte località del mondo come evaporiti. Questi possono essere estratti da cave a cielo aperto o da miniere profonde.
Nella desulfurazione dei gas di scarico, i gas di scarico delle centrali elettriche a combustibili fossili e altri processi (ad esempio la produzione di cemento) vengono lavati per ridurne il contenuto di ossido di zolfo, iniettando calcare o calce finemente macinati. Questi processi di precipitazione tendono a concentrare elementi radioattivi nel solfato di calcio prodotto.
Fino agli anni '70 si producevano quantità commerciali di acido solforico a Whitehaven da solfato di calcio anidro.
Metodo di Preparazione per Impasti
Metodo di preparazione consigliato: versare l'acqua in un contenitore pulito. Il volume dell'acqua deve essere leggermente inferiore al volume dell'impasto già realizzato. Cospargere uniformemente la miscela di gesso nell'acqua fino a quando la miscela non si asciuga più e appare sulla superficie dell'acqua. Mescolare l'impasto fino a renderlo omogeneo. Una volta pronto l'impasto, riempire lo stampo desiderato e lasciare indurire per circa 30 minuti.
Informazioni Tecniche
| Parametro | Proprietà |
|---|---|
| Nome | Solfato di calcio | Gesso di Parigi |
| Sinonimi | Drierite, gesso, plaster of Paris, drierite, gypsum |
| Formula | CaSO4 · ½H2O (Gesso di Parigi) |
| Struttura IUPAC | Solfato di calcio (Calcium sulfate, CI 77231) |
| INCI | CALCIUM SULFATE |
| CAS | 10034-76-1 |
| Massa molare | 145.149 g/mol |
| Densità | 2,211 g/cm³ |
| Solubilità | Poco solubile in glicerolo. In acqua: 0,26 g/100ml a 25 °C |
tags: #solfato #acido #di #calcio