L'ibridazione è un concetto fondamentale in chimica che descrive come gli orbitali atomici di un atomo si combinano per formare nuovi orbitali, detti ibridi, che sono più adatti alla formazione di legami chimici. Questo procedimento di combinazione matematica di un certo numero di orbitali atomici (orbitali s, p) di valenza di un atomo, aventi energie poco diverse, permette di ottenere per quell'atomo altrettanti nuovi orbitali ibridi equivalenti (isoenergetici tra loro, finché possibile), coi lobi orientati lungo le direzioni dettate dalla combinazione matematica stessa. Questi nuovi orbitali ibridi potranno essere usati dall'atomo per formare legami con altri atomi.
Il numero di orbitali ibridi ottenuti è uguale al numero di quelli che vengono combinati, cosicché il numero totale di orbitali di valenza dell'atomo non cambia. L'ibridazione è un modello teorico che aiuta a spiegare la geometria molecolare e la natura dei legami chimici osservati sperimentalmente.
Determinazione del tipo di ibridazione
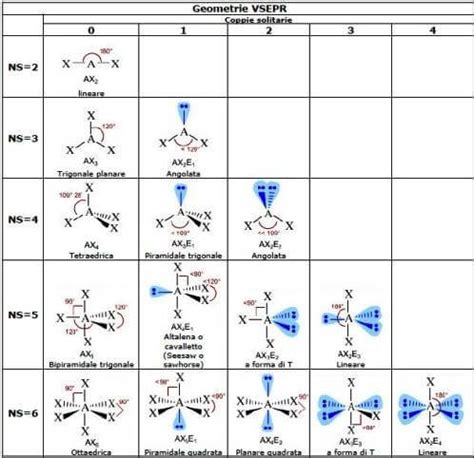
È possibile determinare il tipo di ibridazione dell'atomo centrale di una molecola. Partendo dalla formula di struttura, si contano i legami σ (non quelli π che, legando gli stessi due atomi sono isodirezionali e costituiscono con i precedenti un'unica zona di spazio elettricamente carica, perciò non contano ai fini dell'ibridazione) formati dall'atomo in questione e a questi si aggiungono le coppie solitarie. La somma di questi due valori indica il numero di orbitali atomici necessari per la formazione dei legami e delle coppie solitarie, determinando così il tipo di ibridazione.
Esempi di ibridazione
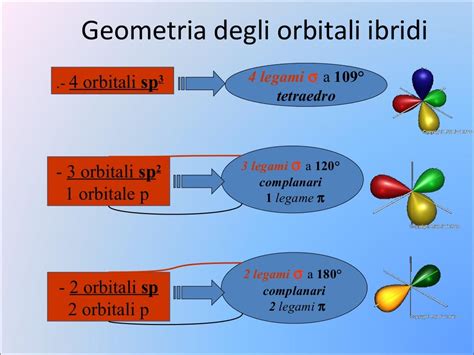
Un esempio comune è l'ibridazione sp3, dove un orbitale s si combina con tre orbitali p per formare quattro orbitali ibridi sp3. Questi orbitali sono diretti verso i vertici di un tetraedro, con un angolo di 109.5° tra di loro. Questa geometria è tipica di molecole come il metano (CH4).
Un altro tipo di ibridazione è l'sp2, in cui un orbitale s si combina con due orbitali p, formando tre orbitali ibridi sp2 giacenti sullo stesso piano e diretti verso i vertici di un triangolo equilatero, con un angolo di 120° tra loro. L'orbitale p rimanente è perpendicolare al piano degli orbitali ibridi e partecipa alla formazione di legami π. Questo tipo di ibridazione si osserva in molecole come l'etilene (C2H4).
L'ibridazione sp, infine, coinvolge la combinazione di un orbitale s con un orbitale p, producendo due orbitali ibridi sp diretti in senso opposto lungo la stessa linea, con un angolo di 180° tra loro. I due orbitali p rimanenti sono perpendicolari tra loro e all'asse degli orbitali sp. L'ibridazione sp è tipica di molecole lineari come l'acetilene (C2H2).
Ibridazione nei complessi metallici
Nel caso di ioni metallici in configurazione elettronica d8, come Ni2+, Pd2+, Pt2+, si può osservare un'ibridazione dsp2. Questo tipo di ibridazione porta alla formazione di quattro legami σ diretti a 90° l'uno dall'altro, verso i vertici di un quadrato. La geometria risultante è planare quadrata.
Se invece questi ioni metallici formano 4 legami σ diretti a 109,5° uno dall'altro, l'ibridazione è sp3. In questo caso, la geometria molecolare è tetraedrica.
Ibridazione orbitali sp, sp2, sp3
Il concetto di ibridazione è cruciale per comprendere la struttura tridimensionale delle molecole e la forza e la natura dei legami chimici che le tengono unite. Permette di spiegare perché certe molecole hanno forme specifiche e come gli atomi interagiscono tra loro per formare composti stabili.
tags: #ibridazione #e #ormani #di #rigore